Impfstoffe dürfen nur dann eingesetzt werden, wenn sie eine staatliche Zulassung besitzen. Um eine möglichst große Verfügbarkeit von Impfstoffen zu sichern, gibt es allerdings einige Ausnahmen, von denen hier die bestandsspezifischen Impfstoffe besprochen werden sollen. Sie dürfen einerseits ohne eine Zulassung hergestellt und eingesetzt werden, unterliegen aber klar definierten Einschränkungen. Folgende Voraussetzungen gelten:
- Für das entsprechende Anwendungsgebiet ist kein Impfstoff zugelassen (Artikel 106 (5) VO2019/6).
- Es wird ein inaktivierter Impfstoff aus einem Erreger oder Erregern aus einem bestimmten Bestand hergestellt (Artikel 2(3) VO 2019/6).
- Dieser Impfstoff darf nur in dem Herkunftsbestand der Erreger (epidemiologische Einheit) oder einem Bestand mit gesicherter epidemiologischer Verbindung eingesetzt werden (Artikel 2(3) VO 2019/6).
Mehr zu aktiven und inaktiven Impfstoffen lesen Sie hier.
Es sind die bereits erwähnte Tierarzneimittel-Verordnung der EU 2019/6 sowie das deutsche Tiergesundheitsgesetz und die Tierimpfstoff-Verordnung zu beachten. Das ebenfalls 2022 in Kraft getretene deutsche Tierarzneimittelgesetz gilt dagegen nicht für Tierimpfstoffe. Eine wichtige Orientierungshilfe bieten die Empfehlungen und Leitlinien der Ständigen Impfkommission Veterinärmedizin beim Friedrich-Loeffler-Institut (https://stiko-vet.fli.de). Besonders zu erwähnen sind die Stellungnahme zur Anwendung bestandsspezifischer Impfstoffe und die Leitlinien zur Impfung von Rindern und kleinen Wiederkäuern.

Vor- und Nachteile
Bemerkenswerte Vorteile von einem bestandsspezifischen Vakzin sind:
- Eine bestehende Lücke bei zugelassenen Impfstoffen zu füllen und damit zugleich auf die spezifische Bestandssituation reagieren zu können.
- Sie können eine sehr zielgenaue Immunisierung gegen die in dem jeweiligen Bestand zirkulierenden Erreger ermöglichen – präzise Diagnostik vorausgesetzt.
Auf der anderen Seite ist die Wirksamkeit solcher Produkte nicht geprüft und kann demzufolge vom Hersteller auch nicht garantiert werden. Auch die für ein Zulassungsverfahren notwendigen umfangreichen Sicherheitsprüfungen können nicht vorliegen. Sie sollten dies also eingehend mit Ihrem Tierarzt besprechen.
Stammauswahl – eine Voraussetzung für die Wirksamkeit
Ein Schritt, der wesentlich über den künftigen Erfolg des Präparates bestimmt, ist die Auswahl des oder der Erregerstämme für die Produktion. Diese Entscheidung kann letztlich nur die bestandsbetreuende Tierärztin unter Berücksichtigung des Krankheitsbildes und der Laborergebnisse treffen. Ein alleiniger Nachweis pathogener Keime im Labor reicht dafür nicht aus, es ist eine Wertung aller Befunde unter Berücksichtigung der Bestandssituation vorzunehmen. Das gilt insbesondere dann, wenn in der Vakzine mehrere Erregerstämme enthalten sein sollen. Für die Laboruntersuchungen sollten im Optimalfall Proben von krankhaften Veränderungen eingesandt werden. Untersuchungsergebnisse von Tupferproben gesunder Tiere sind demgegenüber mit Vorsicht zu interpretieren. Zudem muss der Hersteller eine entsprechende Qualität sichern. Dennoch kann auch damit keine spezielle Wirksamkeit garantiert werden. Eine Bewertung der Wirksamkeit kann erst nach der Anwendung erfolgen und sollte für die künftige Arbeit genutzt werden.
Herstellung
Fragen der Produktion werden nicht im Einzelnen besprochen, dafür sind die jeweiligen pharmazeutischen Unternehmer verantwortlich. Nach der neuen EU-Verordnung 2019/6 sind auch für bestandsspezifische Impfstoffe Regeln der Guten Herstellungspraxis (GMP) anzuwenden.
Das Paul-Ehrlich-Institut informiert auf seiner Website über die Hersteller und die produzierten Mengen (https://www.pei.de). Demnach haben 2019 insgesamt 18 Hersteller 16.681 Chargen bestandsspezifischer Impfstoffe in Deutschland hergestellt, davon waren 3.606 Chargen mit insgesamt 807.085 Impfdosen für Wiederkäuer. In den beiden Vorjahren wurden sogar jeweils mehr als eine Million Impfdosen für Wiederkäuer produziert.

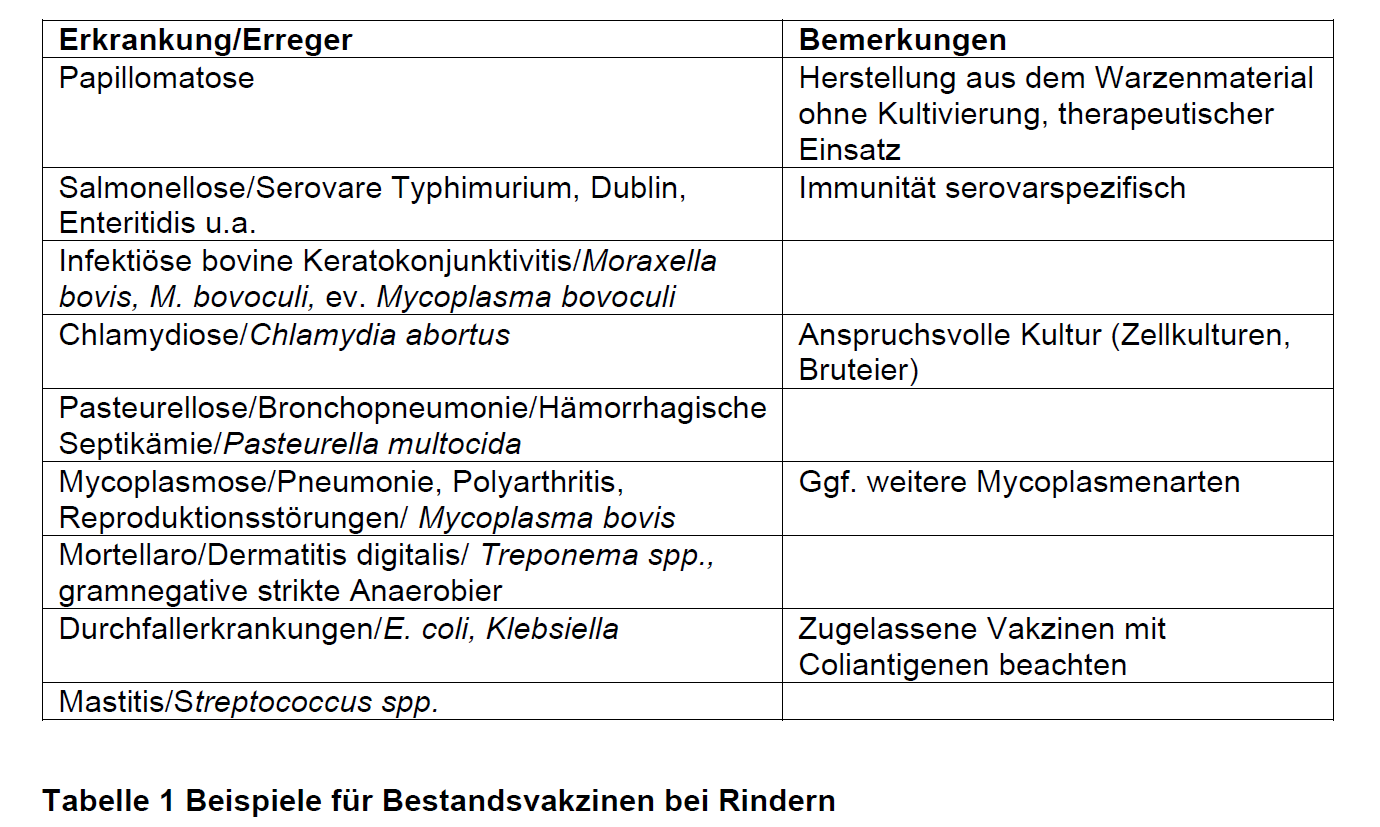
Beispiele für Bestandsvakzinen bei Rindern
Bestandsvakzine können eine relativ breite Palette von Produkten abdecken, wie diese Beispiele in der Tabelle zeigen sollen:
Bestandsspezifische Vakzine unterliegen der tierärztlichen Verschreibungspflicht. Die Verabreichung wird in den meisten Fällen durch subkutane oder intramuskuläre Injektion vorgenommen. Es werden aber auch Vakzine oral (Schluckvakzinen) oder intranasal angewendet. Das betrifft Infektionskrankheiten, für deren Abwehr lokalen Immunmechanismen im Verdauungs- und Atmungstrakt eine besondere Bedeutung zukommt. Auf jeden Fall müssen in diesen Fällen wesentlich höhere Antigendosen verwendet und über jeweils mehrere Tage hintereinander verabreicht werden.
Die Hersteller empfehlen meist die Vortestung eines neuen Produkts an einer kleinen Tiergruppe, um die Reaktion und mögliche Nebenwirkungen abwägen zu können.
Diskussion und Schlussfolgerungen
Diskussionen betreffen immer wieder zwei Punkte, den Begriff des Bestandes und die Verfügbarkeit zugelassener Impfstoffe. Zur Bestandsdefinition enthält die EU-Verordnung 2019/6 im Artikel 2(3) den Begriff der epidemiologischen Einheit. Merkmal dieser Einheit ist nach dem EU-Tiergesundheitsrechtsakt (VO 2016/429 Artikel 4 Nr. 39) die gleiche Wahrscheinlichkeit für die Tiere, einem Seuchenerreger ausgesetzt zu sein. Eine sehr wichtige Ergänzung wird im Artikel 2(3) der Tierarzneimittelrichtlinie mit der Beschreibung der „…gesicherten epidemiologischen Verbindung…“ zwischen verschiedenen Einheiten („Beständen“) gemacht. Das kann beispielsweise bei Lieferung von Tieren von einem Bestand A in einen Bestand B relevant werden. Wenn in dem Bestand B relativ kurze Zeit nach der Ankunft der Tiere Infektionen auftreten, kommt eine Impfung bei Ankunft in dem Bestand zu spät. Dann kann es sinnvoll sein, bereits im Herkunftsbestand einen Impfstoff mit Erregern aus dem Zielbestand B einzusetzen, sofern die gesicherte epidemiologische Verbindung nachgewiesen werden kann.
Das zweite Thema ist das Vorhandensein einer zugelassenen Vakzine. Hier kann es nicht nur allein um die Erregerart gehen, sondern es müssen die in der Zulassung der Vakzine angegebenen Anwendungsgebiete geprüft werden. Sie können sich auf bestimmte Typen des Erregers mit bestimmten Merkmalen beschränken und somit die Anwendung anderer Varianten in einer Bestandsvakzine durchaus möglich machen. Dies muss aber unter Berücksichtigung der Pathogenese der jeweiligen Infektionskrankheit belegt werden.
Zusammenfassend können bestandsspezifische Impfstoffe als Mittel zur Schließung von Lücken in der Impfstoffpalette bewertet werden. Ihr Einsatz erfordert ein spezifisches Eingehen auf die Erregersituation der jeweiligen Bestände und eine gute Zusammenarbeit zwischen Tierärzten, Tierhaltern, diagnostischen Einrichtungen und Herstellern.
Dieser Text stammt von Prof. Dr. med. vet. habil. Hans-Joachim Selbitz, Leipzig und ist in Kooperation mit www.milchpraxis.de entstanden. 
